Le sommeil paradoxal (SP), cet état fascinant où notre esprit s'évade dans le monde des rêves, est un phénomène qui a longtemps intrigué l'humanité. Caractérisé par une activité cérébrale intense, similaire à celle de l'éveil, paradoxalement associée à une atonie musculaire généralisée, le SP est un pilier de notre vie nocturne. Cette paralysie musculaire n'est pas anodine ; elle nous protège des mouvements potentiellement dangereux issus de nos rêves, comme en témoigne le syndrome d'Antonio et de marche en sommeil paradoxal (SAMS), où cette atonie fait défaut, permettant aux individus de réaliser des actions complexes et parfois violentes durant leur sommeil.
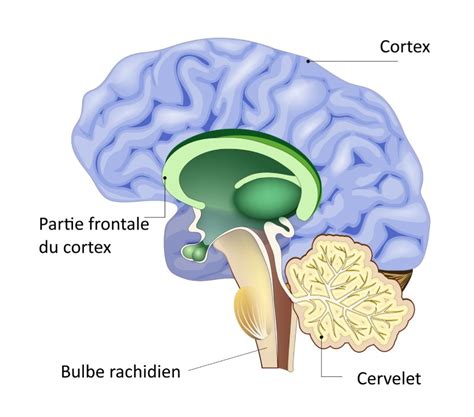
Le Pont et le Bulbe Rachidien : Des Structures Clés dans la Régulation du Sommeil Paradoxal
Au cœur de ce mécanisme se trouvent des régions cérébrales spécifiques, notamment le pont et le bulbe rachidien (ou moelle allongée). Le pont, une partie centrale et renflée du tronc cérébral, située entre le mésencéphale et la moelle allongée, joue un rôle crucial. Anatomiquement, il se positionne en arrière du cervelet et en avant de la moelle allongée, dont il est séparé par le sillon bulbopontique. Sa face antérieure est traversée par le sillon basilaire, tandis que sa face postérieure forme le plancher du quatrième ventricule. Contrairement à d'autres parties du tronc cérébral, le pont est majoritairement constitué de fibres nerveuses transverses, dont une proportion significative forme les fibres pontocérébelleuses, reliant le cortex au cervelet via les pédoncules cérébelleux moyens.
Le bulbe rachidien, quant à lui, est la partie terminale du tronc cérébral, prolongeant le pont vers la moelle épinière. Il abrite des structures vitales pour le contrôle de fonctions automatiques telles que la respiration et la pression artérielle, mais il est également impliqué dans la régulation du sommeil. Des formations anatomiques comme les pyramides médullaires, les olives inférieures, les noyaux des nerfs crâniens (IX à XII) et la formation réticulée y sont présentes.
Le Générateur de l'Atonie : Le Noyau Sublatérodorsal (SLD)
Des recherches approfondies ont permis d'identifier le noyau sublatérodorsal (SLD), une petite région du pont dorsal, comme le principal générateur de l'atonie musculaire caractéristique du sommeil paradoxal. Composé de neurones glutamatergiques excitateurs, le SLD joue un rôle central dans l'inhibition des motoneurones spinaux, ces unités fonctionnelles contrôlant l'activité musculaire.
Bien-être : Importances du sommeil paradoxal et profond
Les Neurones Inhibiteurs : Glycine et GABA au Service de l'Atonie
Le mécanisme précis par lequel le SLD induit l'atonie a fait l'objet d'intenses recherches. Il est désormais admis que, pendant le SP, le SLD exerce son influence inhibitrice sur les motoneurones spinaux via l'activation de neurones inhibiteurs contenant de la glycine et du GABA (acide gamma-aminobutyrique). Ces neurotransmetteurs inhibiteurs provoquent une hyperpolarisation des motoneurones, les rendant moins susceptibles de s'activer et donc de générer des mouvements musculaires.
Un débat scientifique de longue date a porté sur la localisation de ces neurones inhibiteurs : se trouvent-ils dans le bulbe rachidien ou directement dans la moelle épinière ? Des études récentes, combinant des techniques d'anatomie fonctionnelle et des marqueurs moléculaires chez le rat, ont apporté une réponse claire. Elles démontrent que la partie ventro-médiane du bulbe rachidien (vmM) héberge une population de neurones glycinergiques qui sont spécifiquement recrutés pendant le SP et projettent vers les motoneurones lombaires. Bien que des neurones glycinergiques soient également présents dans la moelle épinière, leur activation durant le SP est négligeable, excluant ainsi leur contribution majeure à l'atonie.
Preuve Fonctionnelle : Suppression de la Transmission Inhibitrice dans la vmM
Pour confirmer le rôle fonctionnel des neurones inhibiteurs de la vmM, des expériences ont été menées en utilisant des vecteurs viraux (AAV) pour bloquer l'expression du vGAT (transporteur vésiculaire du GABA et de la glycine). Cette suppression génétique de la transmission inhibitrice issue de la vmM chez le rat a eu des conséquences notables. Bien que le comportement à l'éveil soit normal, la durée des épisodes de SP a été réduite. Plus significativement, l'analyse électromyographique a révélé une augmentation du tonus musculaire pendant le SP, remplaçant l'atonie caractéristique. Cette persistance du tonus a facilité l'exécution de mouvements complexes durant le sommeil onirique, reproduisant ainsi des symptômes observés chez les patients atteints du SAMS.
Ces résultats convergent pour souligner le rôle crucial des neurones inhibiteurs de la vmM dans l'expression de l'atonie du SP. La perte de fonction de ces neurones est suffisante pour maintenir un tonus musculaire durant le SP et favoriser des comportements oniriques anormaux.
Lien avec les Maladies Neurodégénératives : Le SAMS et la Maladie de Parkinson
L'importance de ces découvertes dépasse la compréhension fondamentale du sommeil. Le SAMS est reconnu comme le meilleur marqueur diagnostique précoce de la maladie de Parkinson (MP), avec une fenêtre temporelle d'une dizaine d'années. Une théorie actuelle propose que le SAMS soit causé par une α-synucléinopathie, une accumulation anormale de la protéine α-synucléine, qui affecterait initialement les aires cérébrales responsables de l'atonie. Cette pathologie se propagerait ensuite au fil des années à d'autres régions du cerveau, conduisant ultimement au développement de la MP.
Les modèles animaux de SAMS, tels que ceux obtenus par inactivation génétique du SLD ou de la vmM, offrent des outils précieux pour explorer les mécanismes physiopathologiques sous-jacents et développer de nouvelles stratégies thérapeutiques. Des études anatomo-pathologiques ont d'ailleurs mis en évidence des processus inflammatoires ou lésionnels dans des régions cérébrales correspondant au SLD et à la vmM chez des patients atteints de SAMS, soutenant ainsi l'hypothèse d'une atteinte précoce de ces réseaux dans le cadre de la neurodégénérescence.
Le Réseau Neuronal de l'Atonie : Une Cascade d'Événements
Le modèle neuronal proposé pour expliquer l'atonie durant le SP implique une cascade d'événements :
- Activation du SLD : Dès l'entrée en SP, les neurones glutamatergiques du SLD s'activent.
- Excitation des neurones inhibiteurs de la vmM : Via leurs projections descendantes, les neurones du SLD excitent les neurones GABA/glycine de la vmM.
- Inhibition des motoneurones spinaux : Les neurones de la vmM, en libérant du GABA et de la glycine, inhibent les motoneurones spinaux, induisant l'atonie musculaire.
Ce réseau, bien que restreint au tronc cérébral inférieur dans sa fonction d'induction de l'atonie, pourrait être la cible précoce d'une attaque α-synucléinopathique. La propagation lente de cette pathologie à travers les voies d'interconnexion cérébrales, potentiellement via un mécanisme de transmission de cellule à cellule, expliquerait le développement progressif des symptômes moteurs de la maladie de Parkinson.
Implications et Perspectives
La compréhension fine des neurones cholinergiques, mais aussi glutamatergiques, GABAergiques et glycinergiques du tronc cérébral, et de leur rôle dans la régulation de l'atonie pendant le sommeil paradoxal, ouvre des perspectives considérables. Elle éclaire non seulement les mécanismes fondamentaux du sommeil et du rêve, mais offre également des pistes prometteuses pour le diagnostic précoce et le traitement de maladies neurodégénératives dévastatrices comme la maladie de Parkinson. L'identification précise des régions cérébrales impliquées dans l'atonie, et potentiellement endommagées dans le SAMS et la MP, constitue une étape essentielle dans la quête de nouvelles thérapies neuroprotectrices.