La conversion de la biomasse lignocellulosique en produits biochimiques, biomatériaux et bioénergies représente un domaine d'intérêt croissant, et la cellulase y joue un rôle crucial. Pour faciliter la récupération et la réutilisation de cette enzyme après réaction, l'immobilisation sur des matrices insolubles a été privilégiée par le passé. Cependant, cette approche peut entraîner un contact insuffisant entre l'enzyme et le substrat, particulièrement lorsque des substrats cellulosiques insolubles sont utilisés. L'utilisation de matrices intelligentes dites « S-IS » (soluble-insoluble) pour l'immobilisation de la cellulase offre une solution prometteuse en créant un biocatalyseur intelligent. Ce biocatalyseur combine les avantages d'un catalyseur homogène, réduisant les résistances de transfert de masse, et d'un catalyseur hétérogène, permettant une récupération aisée.
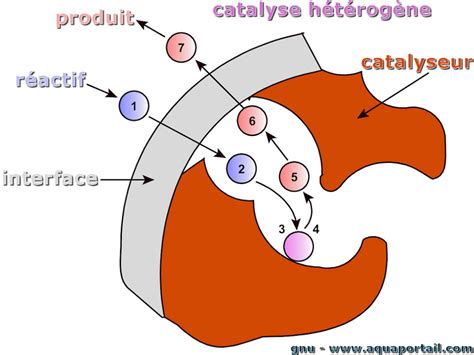
L'Eudragit L-100, un polymère intelligent couramment employé, a été étudié pour l'immobilisation de la cellulase via un couplage carbodiimide. Ce polymère est un copolymère d'acide méthacrylique et de méthacrylate de méthyle, riche en groupes carboxyle. L'activation de ces groupes par un carbodiimide permet la liaison de la cellulase. Cependant, les immobilisations antérieures, notamment en présence d'acétate, conduisaient à une immobilisation non covalente, résultant en un rendement d'activité relativement faible et une réutilisabilité insatisfaisante. Pour pallier ces limitations, cette étude a exploré l'immobilisation de la cellulase sur l'Eudragit L-100 en l'absence d'acétate et avec l'ajout de N-hydroxysuccinimide (NHS) pour améliorer le couplage carbodiimide.
Une observation préliminaire a révélé que la cellulase immobilisée présentant une activité élevée sur le papier filtre ne montrait pas une capacité d'hydrolyse proportionnellement forte sur la biomasse lignocellulosique complexe comme la paille, l'herbe et le bois. Cette divergence est probablement due aux différences structurelles et compositionnelles des substrats enzymatiques. Alors que le papier filtre est essentiellement de la cellulose pure, la biomasse lignocellulosique est un composite de lignine, cellulose et hémicellulose. Dans des applications pratiques, le substrat enzymatique est cette biomasse complexe. Par conséquent, dans cette étude, le glucose produit par l'hydrolyse d'une biomasse lignocellulosique par la cellulase immobilisée a été utilisé comme indicateur clé (réponse) pour optimiser les conditions d'immobilisation. Une production accrue de glucose reflète une plus grande capacité hydrolytique de la cellulase immobilisée et donc une efficacité d'immobilisation plus élevée.
Les techniques d'optimisation basées sur des modèles gagnent en popularité car elles permettent d'analyser les interactions combinées de chaque facteur, tout en étant plus économes en main-d'œuvre que les approches « un facteur à la fois ». La méthodologie des surfaces de réponse (RSM) est fréquemment utilisée et a démontré son efficacité dans l'optimisation de procédés multi-facteurs, en particulier pour les systèmes à trois facteurs. Cependant, la RSM présente des limites dans la simulation de données issues de domaines expérimentaux irréguliers et ne peut simuler que des comportements non linéaires d'ordre inférieur dans des régions expérimentales régulières. En contraste, les réseaux de neurones artificiels (ANN), une autre approche de modélisation, ne souffrent pas de ces limitations liées à la conception expérimentale et nécessitent relativement moins d'expériences pour une simulation efficace. Récemment, les ANN ont démontré une précision de simulation et de prédiction supérieure à celle de la RSM dans la modélisation de nombreuses réactions biochimiques. De plus, une valeur d'optimisation plus élevée et plus précise est généralement obtenue avec la combinaison ANN et algorithme génétique (GA) par rapport à la RSM. L'algorithme génétique (GA) est un autre outil d'intelligence artificielle qui exploite les processus de sélection par évolution naturelle, aboutissant à la survie des espèces les mieux adaptées.
Dans la lignée de nos travaux antérieurs, deux techniques d'intelligence artificielle, les ANN et les GA, ont été combinées pour optimiser l'immobilisation de la cellulase sur l'Eudragit L-100.
Simulation et Prédiction Basées sur les Réseaux de Neurones Artificiels (ANN)
Après un nombre limité d'essais expérimentaux, l'objectif d'apprentissage a été atteint, permettant la construction réussie d'un réseau de neurones artificiels (ANN). L'efficacité d'immobilisation ajustée par l'ANN est présentée dans le Tableau 1. Ce tableau met en évidence la quasi-identité entre les valeurs expérimentales et les valeurs simulées par l'ANN. Les indicateurs d'évaluation de la performance de simulation de l'ANN, tels que l'erreur absolue/relative moyenne, l'erreur quadratique moyenne et la variance, étaient respectivement de 0,74, 1,18 %, 0,99 et 0,98. Ces valeurs remarquablement faibles confirment la très haute précision de l'ajustement. Des résultats similaires ont été observés dans d'autres bioprocédés utilisant des ajustements basés sur les ANN.
L'analyse de variance (ANOVA) présentée dans le Tableau 2 confirme la significativité du modèle ANN, comme l'indiquent les valeurs de F et de P. Le coefficient de corrélation entre les données expérimentales et simulées est supérieur à 0,99, une valeur très proche de 1, attestant de la perfection de l'ajustement.
Pour valider le réseau ANN entraîné, trois expériences supplémentaires ont été réalisées (essais 21 à 23 dans le Tableau 1). Les résultats expérimentaux se sont avérés très proches des prédictions basées sur l'ANN, avec des erreurs relatives entre les valeurs expérimentales et prédites inférieures à 3,0 %. Ces excellents résultats d'ajustement et de prédiction démontrent le succès de l'entraînement de l'ANN, le rendant apte à servir de fonction de désirabilité entre l'efficacité d'immobilisation et les trois facteurs étudiés.
Optimisation par Algorithme Génétique (GA) Basée sur l'ANN
Une fois le réseau ANN construit avec succès, l'algorithme génétique (GA) a été employé pour rechercher la valeur maximale de l'efficacité d'immobilisation. Les résultats de 50 simulations stochastiques indiquent que la plage de la fonction objectif maximale se situe entre 84,23 % et 89,76 %, avec des valeurs minimales et moyennes allant de 40,28 % à 48,96 % et de 78,23 % à 80,99 %, respectivement. La valeur moyenne de la fonction objectif maximale calculée est de 88,76 %, ce qui représente la valeur optimisée obtenue par les techniques d'intelligence artificielle combinées (ANN-GA). Les conditions optimisées correspondantes sont une concentration d'EDC de 0,44 %, une concentration de NHS de 0,37 % et un temps de couplage de 2,22 heures. L'efficacité d'immobilisation déterminée expérimentalement dans ces conditions était de 87,97 ± 6,45 %, démontrant un accord parfait avec l'optimisation ANN-GA (déviation inférieure à 1 %). Des résultats similaires ont été rapportés pour d'autres bioprocédés.
La Figure 2 illustre l'évolution de l'algorithme au fil des générations. Partant d'une efficacité moyenne de 61,36 %, celle-ci augmente progressivement jusqu'à la 7ème génération pour atteindre 86,33 % à la fin des 50 générations. L'efficacité d'immobilisation maximale a également montré une augmentation notable au cours des premières générations, atteignant 88,76 % à la 22ème génération avant de se stabiliser.
Comparativement à la RSM, l'intelligence artificielle offre une capacité supérieure à modéliser la non-linéarité, une simulation et une prédiction plus précises, permettant ainsi d'obtenir une meilleure optimisation. De plus, l'IA ne souffre pas des limitations inhérentes à la conception expérimentale, et une simulation efficace requiert un nombre d'expériences relativement réduit. Bien entendu, la précision peut être accrue avec un plus grand nombre d'expériences pour capturer des comportements non linéaires plus complexes. Par conséquent, avec l'IA, un espace de recherche plus libéral peut être choisi, même si la corrélation dans cet espace est plus complexe que celle décrite par une équation de degré supérieur.
Réutilisabilité
La cellulase immobilisée a été mélangée avec le substrat insoluble sous agitation. Après réaction, le substrat non dégradé était filtré ou précipité par centrifugation. Le surnageant obtenu était ensuite acidifié pour abaisser le pH, puis centrifugé. Le précipité obtenu correspondait à la cellulase immobilisée recyclée, prête pour l'hydrolyse suivante. Conformément à nos rapports précédents, plus de 50 % de la productivité initiale est conservée après cinq réutilisations, soulignant la durabilité de la méthode d'immobilisation.
Section Expérimentale
Matériaux
L'Eudragit L-100, un copolymère d'acide méthacrylique et de méthacrylate de méthyle, est un polymère soluble en solution aqueuse à un pH supérieur à 4,3. Ce pH critique de solubilité est déplacé à 5,0 après couplage avec la cellulase. La cellulase, avec une activité de 74,07 FPU/g (Unité d'Activité de Filtre à Papier), a été fournie par Novozymes (Bagsværd, Danemark). Le blé broyé, obtenu d'une ferme locale, a été prétraité alcalinement selon la méthode décrite par Carrillo et al. Les réactifs 1-Éthyl-3-(3-diméthylaminopropyl) carbodiimide (EDC) et N-hydroxysuccinimide (NHS) ont été obtenus auprès de Sigma-Aldrich (St. Louis, MO, USA) et de Shanghai Aladdin Biochemical Technology Co., Ltd. (Shanghai, Chine), respectivement.
Immobilisation de la Cellulase sur Eudragit L-100
L'immobilisation covalente de la cellulase sur l'Eudragit L-100 a été réalisée par couplage carbodiimide en présence de NHS, en suivant un protocole adapté. Une solution de 50 mL d'Eudragit L-100 (2 %, p/v) a été préparée comme décrit par Sardar et al. Pour activer le polymère, du NHS (0,08 %-0,48 %, p/v) et de l'EDC (0,06 %-0,74 %, p/v) ont été ajoutés successivement. Après 15 minutes de mélange, 100 mg de protéine de cellulase brute ont été ajoutés et le mélange a été agité pendant 0,48 à 5,52 heures. La plage de temps choisie était basée sur une étude antérieure où le temps de couplage optimal en l'absence de NHS était d'environ 3 heures. Le pH du mélange a été ajusté à 3,6 avec de l'acide acétique glacial. Les précipités ont été séparés par centrifugation (6800 × g, 10 min) à 4,0 °C et lavés trois fois avec de l'acide acétique 0,02 mol/L. Enfin, les précipités ont été redissous dans 50 mL de tampons acétate (0,2 mol/L, pH 5,0) et utilisés comme cellulase immobilisée pour les expériences d'hydrolyse ultérieures.
Plan d'Expériences Composite Central (CCD)
L'Eudragit L-100, un copolymère d'acide méthacrylique et de méthacrylate de méthyle, possède de nombreux groupes carboxyle qui sont utilisés comme groupes fonctionnels privilégiés pour le couplage de la cellulase. L'EDC est un agent d'activation des carboxyles couramment utilisé pour former des liaisons amide avec les amines primaires, et le NHS peut améliorer ce couplage. Outre l'EDC (agent de couplage) et le NHS (agent d'amélioration), le temps de couplage est également un facteur important influençant la réaction entre l'Eudragit L-100 et la cellulase. Un temps insuffisant peut entraîner un couplage incomplet de la cellulase, tandis qu'un temps excessif pourrait conduire à un sur-couplage affectant négativement le site actif de l'enzyme. Ainsi, dans cette étude, la concentration d'EDC (X1), la concentration de NHS (X2) et le temps de couplage (X3) ont été définis comme variables indépendantes (entrées de l'ANN). Un plan d'expériences composite central (CCD) pour les trois facteurs a été appliqué pour entraîner l'ANN. La plage et les niveaux de chaque facteur sont présentés dans le Tableau 3. Le CCD comprenant 20 essais (dont six points centraux) était basé sur un plan factoriel complet 2³ à une distance de 1,68 de l'origine (essais 1 à 20 dans le Tableau 1).
Réseau de Neurones Artificiels (ANN)
Un réseau de neurones artificiels (ANN) est une architecture de programme informatique capable de calculs non linéaires dans certaines configurations, comme le perceptron multicouche (MLP). Il peut identifier des fonctions discriminantes arbitraires directement à partir de données expérimentales. Dans notre expérimentation, l'architecture de l'ANN comprenait trois neurones (concentration d'EDC X1, concentration de NHS X2 et temps de couplage X3) dans la couche d'entrée, quatre neurones dans la couche cachée, et un neurone (efficacité d'immobilisation) dans la couche de sortie. Ceci représente une architecture de réseau neuronal typique.
Les formules suivantes décrivent la mise à l'échelle des données pour les couches d'entrée et de sortie :
$Xi^* = \frac{Xi - X{min}}{X{max} - X_{min}}$
$Y^* = \frac{Y - Y{min}}{Y{max} - Y_{min}}$
où $X_i^$ et $Y^$ sont les nouvelles données mises à l'échelle des couches d'entrée et de sortie, respectivement.
L'algorithme de rétropropagation, le plus fréquemment utilisé, a servi à entraîner un modèle ANN aléatoire en alimentant les données nouvellement mises à l'échelle. Cet algorithme comprend la propagation avant du signal et la rétropropagation de l'erreur.
La formule pour la couche cachée est :
$Zj = f(\sum{i=1}^{n} w{ij}Xi^* - b_j)$
où $Zj$ sont les données de la couche cachée, $w{ij}$ sont les poids de connexion de $Xi^*$ à $Zj$, et $b_j$ est le biais de la couche cachée.
Pour la couche de sortie :
$Y{pred}^* = f(\sum{j=1}^{m} w{jk}Zj - b_k)$
où $Y{pred}^$ est la sortie prédite mise à l'échelle, $w{jk}$ sont les poids de connexion de $Zj$ à $Y{pred}^$, et $b_k$ est le biais de la couche de sortie.
Les fonctions de transfert utilisées dans les couches cachée et de sortie de l'ANN étaient respectivement des fonctions sigmoïde tangentielle et linéaire pure. L'erreur quadratique moyenne entre les résultats des neurones de sortie et les sorties réelles était calculée et rétropropagée à travers le réseau. L'algorithme ajustait ensuite le poids de chaque connexion. Une fois l'erreur quadratique moyenne atteinte 10⁻⁴, l'entraînement était terminé et l'ANN correspondant était construit. Toutes les procédures ont été réalisées à l'aide de Matlab 7.1.
Algorithme Génétique (GA)
En utilisant l'ANN entraîné comme fonction de fitness, un algorithme génétique (GA) a été couplé pour rechercher le maximum de l'efficacité d'immobilisation. L'objectif est de trouver un vecteur de variables de décision, c'est-à-dire les neurones d'entrée de l'ANN ($X_i$), afin de maximiser la fonction objectif, c'est-à-dire la sortie de l'ANN. Les paramètres de fonctionnement tels que le nombre total de générations, la taille de la population, le nombre de variables codées en binaire, la probabilité de croisement et la probabilité de mutation étaient respectivement de 50, 20, 3, 0,4 et 0,005.
L'algorithme génétique utilise des processus de sélection par évolution naturelle, où la sélection aboutit aux individus les mieux adaptés. Une population d'individus est maintenue à chaque génération, et chaque individu représente une solution potentielle au problème. L'individu choisi dans cette étude était un ensemble de valeurs pour la concentration d'EDC (X1), la concentration de NHS (X2) et le temps de couplage (X3). La recherche d'une solution optimale par GA commence par une population initialisée aléatoirement de solutions candidates. Ces candidats sont appelés chaînes ou chromosomes. Chaque chromosome est évalué pour mesurer sa fitness à l'aide du modèle basé sur l'ANN. Les étapes impliquées dans l'algorithme d'optimisation basé sur GA sont les suivantes :
- Génération aléatoire d'une population d'individus et attribution d'une valeur de fitness à chaque individu pour guider la recherche par une fonction de fitness spécifique.
- Sélection des individus présentant les valeurs de fitness les plus élevées et leur soumission à des opérations génétiques, incluant le croisement et la mutation.
- Utilisation de la nouvelle population générée comme population parente pour la génération suivante et application continue du même processus évolutif jusqu'à ce qu'un critère d'arrêt soit satisfait.
L'algorithme a été exécuté 50 fois dans cette étude. Toutes les procédures ont été réalisées à l'aide de Matlab 7.1.
Détermination de l'Efficacité d'Immobilisation
Avant et après l'immobilisation, 100 mg de protéine de cellulase ont été incubés avec 2,5 g de blé broyé prétraité à pH 5,0, 50 °C et 120 tr/min. La charge solide était de 5 % (p/v). Après 12 heures, un échantillon de la solution a été prélevé et centrifugé à 4000 tr/min et 4 °C pendant 5 minutes. Le surnageant obtenu a été chauffé à 80 °C pendant 10 minutes puis utilisé pour le dosage du glucose.
Méthode HPLC
Le glucose a été déterminé par un système HPLC Waters 2695 comprenant un contrôleur de système Waters 600E, un injecteur automatique Waters 717, une colonne C18 et un détecteur UV à 210 nm.
Discussion sur les Méthodes de Couplage Covalent
Le couplage covalent de biomolécules, en particulier d'anticorps ou de fragments d'anticorps, à des surfaces ou des nanoparticules est une étape fondamentale dans la fabrication de biocapteurs, de systèmes d'administration de médicaments et d'autres dispositifs biomédicaux. La méthode EDC/NHS est une stratégie largement utilisée pour activer les groupes carboxyle présents sur une surface ou une molécule, permettant leur réaction avec les groupes amine primaires d'une autre molécule, comme les anticorps. Cette chimie est particulièrement utile pour l'immobilisation d'anticorps sur des nanoparticules fonctionnalisées avec des groupes carboxyle, comme les nanoparticules d'or (AuNPs) stabilisées par du citrate ou de l'L-asparagine.
Dans le contexte de la fabrication de biocapteurs, l'immobilisation orthogonale des anticorps est cruciale pour garantir une orientation spécifique et maximiser la disponibilité des sites de liaison antigénique, ce qui se traduit par une sensibilité accrue. Une étude comparative a évalué différentes stratégies d'immobilisation d'anticorps anti-CA125 sur des électrodes modifiées par des nanoparticules d'or. L'immobilisation après activation EDC-NHS des nanoparticules d'or stabilisées par du citrate a montré une sensibilité de 147,53 Ω/(IU/mL)/cm². En comparaison, l'immobilisation directe sur des nanoparticules d'or stabilisées par de l'L-asparagine a résulté en une sensibilité de 166,24 Ω/(IU/mL)/cm² pour la deuxième stratégie et une impressionnante sensibilité de 349,36 Ω/(IU/mL)/cm² pour la troisième stratégie. De plus, une gamme dynamique étendue de 0 à 750 UI/mL a été observée avec la troisième stratégie, contre 500 UI/mL pour les autres. Ces résultats suggèrent que la stabilisation par l'L-asparagine et l'immobilisation directe pourraient favoriser une orientation plus favorable de l'anticorps, conduisant à une performance de biocapteur améliorée.
Une autre application concerne la conjugaison de nanobâtonnets d'or (GNRs) avec des agonistes de récepteurs pro-apoptotiques (PARAs), des anticorps ou des ligands contenant des fragments Fc. L'objectif est de créer des agents antitumoraux sélectifs. Les GNRs peuvent être fonctionnalisés via des méthodes telles que EDC/NHS, la condensation aldéhyde-amine suivie de la réduction de la base de Schiff, ou la chimie click orientée médiatisée par DBCO. L'étape initiale implique le greffage de PEG10K pour la monodispersité des GNRs et la chimie appropriée avant le couplage des PARAs. Bien que la méthode EDC/NHS soit efficace pour conjuguer des ligands Fc ou des anticorps anti-DR4 aux GNRs, le potentiel pro-apoptotique était le mieux conservé avec la chimie click, qui a amplifié le potentiel pro-apoptotique de l'anticorps anti-DR4.
Le couplage carbodiimide, impliquant l'EDC et le NHS, est une méthode polyvalente pour l'activation des groupes carboxyle afin de former des liaisons amide avec les groupes amine primaires. Ce processus est couramment utilisé pour l'étiquetage, le réticulation et l'immobilisation de biomolécules. L'EDC, en particulier, est soluble dans l'eau et est largement utilisé pour les applications en milieu aqueux. Il réagit avec les groupes carboxyle pour former un intermédiaire O-acylisourée, qui est ensuite attaqué par un groupe amine primaire pour former une liaison amide. L'ajout de NHS ou de Sulfo-NHS améliore l'efficacité de cette réaction et permet la formation d'intermédiaires NHS-ester, plus stables et réactifs avec les amines primaires, même à pH physiologique.
Le DCC (dicyclohexylcarbodiimide) fonctionne de manière similaire à l'EDC mais est insoluble dans l'eau, le rendant plus adapté aux synthèses organiques et aux applications industrielles plutôt qu'aux laboratoires de recherche biologique typiques. La plupart des réactifs d'étiquetage et de réticulation NHS-ester commercialement disponibles sont fabriqués à l'aide du DCC.
Dans le domaine de la protéomique, des techniques d'immunoaffinité basées sur la spectrométrie de masse, utilisant des peptides contenant des motifs spécifiques, ont été développées. Ces approches peuvent impliquer l'immobilisation de ligands ou d'anticorps sur des supports solides pour la purification sélective de peptides cibles.
L'immobilisation de peptides sur des supports solides, tels que la résine d'agarose CarboxyLink, est une autre application importante de la chimie carbodiimide. La résine est fonctionnalisée avec des groupes amine qui réagissent avec les groupes carboxyle des peptides, permettant leur attachement pour des applications telles que la purification par affinité d'anticorps.
Les vésicules extracellulaires (EVs) suscitent un intérêt croissant en tant que biomarqueurs potentiels. Leur ciblage, isolation et caractérisation sont cependant difficiles en raison de leur présence dans des échantillons biologiques complexes. L'utilisation de nanoparticules hybrides (NPs), telles que les NPs d'oxyde de fer superparamagnétique (SPIONs) et les NPs d'or (AuNPs), fonctionnalisées avec des ligands spécifiques, vise à faciliter le ciblage et la caractérisation des EVs. Ces NPs peuvent être biofonctionnalisées avec des anticorps pour cibler des biomarqueurs d'intérêt sur des microparticules polymères biomimétiques servant de modèles d'EVs. La spectroscopie de surface plasmon résonance (SPR) est utilisée pour évaluer la capacité de ciblage des NPs biofonctionnalisées.
Dans le domaine de l'immunothérapie, des projets explorent l'utilisation de NPs hybrides pour cibler les récepteurs de mort de la superfamille du facteur de nécrose tumorale (TNF) et induire l'apoptose des cellules cancéreuses, souvent en combinaison avec l'hyperthermie. Des nanorods d'or (AuNRs) sont synthétisés et fonctionnalisés avec des PEG hétérobifonctionnels pour améliorer leur stabilité et réduire la cytotoxicité. Différentes stratégies de couplage, y compris l'EDC/NHS, la formation de base de Schiff et la chimie click, sont évaluées pour greffer des biomolécules aux AuNRs. La chimie click s'est avérée particulièrement efficace pour maximiser les effets pro-apoptotiques dans ce contexte.
Les anticorps, en tant que molécules complexes composées de chaînes lourdes et légères, sont des outils thérapeutiques et diagnostiques puissants. L'ingénierie génétique a permis de créer divers formats d'anticorps, tels que les anticorps chimérisés, humanisés, bispécifiques et multivalents, afin d'améliorer leur efficacité et de réduire leur immunogénicité. Ces formats d'anticorps peuvent être produits à partir de constructions plasmidiques et trouvent des applications dans le traitement et le diagnostic de diverses pathologies, notamment le cancer. Les domaines variables de camélidés (VHH) ont également émergé comme des fragments d'anticorps prometteurs en raison de leur petite taille et de leur grande stabilité, permettant la conception de formats d'anticorps innovants.
Le développement de vecteurs d'expression, tels que des plasmides, est essentiel pour la production de ces formats d'anticorps modifiés. Ces plasmides intègrent des séquences d'ADN codant pour les domaines d'anticorps spécifiques, les régions constantes d'immunoglobulines humaines, et d'autres éléments nécessaires à leur expression fonctionnelle dans des systèmes d'expression bactérienne ou mammifère. Les techniques de biologie moléculaire, telles que la PCR, la digestion par enzymes de restriction, la ligature et la transformation, sont utilisées pour construire et manipuler ces plasmides.
L'isolement de fragments d'anticorps spécifiques, comme les VHH, à partir de banques génomiques ou de bibliothèques générées par phage-display, est une étape clé. La technologie du phage-display permet de cribler de vastes collections de fragments d'anticorps pour identifier ceux qui se lient spécifiquement à une cible d'intérêt. Les VHH isolés peuvent ensuite être produits en grande quantité dans des systèmes d'expression bactérienne après clonage dans des vecteurs d'expression appropriés.
En résumé, l'optimisation de l'immobilisation de biomolécules, qu'il s'agisse d'enzymes ou d'anticorps, repose sur une compréhension approfondie des chimies de couplage disponibles et sur l'application de techniques d'optimisation avancées. Les méthodes basées sur l'intelligence artificielle, comme les ANN et les GA, offrent des outils puissants pour explorer de manière systématique et efficace les paramètres d'optimisation, conduisant à des performances améliorées dans diverses applications biotechnologiques. La comparaison des différentes stratégies de couplage, telles que EDC/NHS, chimie click, et l'immobilisation directe, est essentielle pour sélectionner la méthode la plus appropriée en fonction de l'application visée et des caractéristiques des biomolécules et des supports utilisés.