La collection de souches fongiques du Muséum National d'Histoire Naturelle (MNHN) représente une ressource inestimable pour la recherche scientifique, abritant une diversité remarquable de champignons essentiels à de nombreux domaines d'étude. Cette collection, qui compte aujourd'hui plus de 6 000 souches, dont 350 types, et couvre 1 425 espèces différentes, est particulièrement axée sur les Ascomycètes et les Zygomycètes, des organismes souvent saprophytes et impliqués dans les environnements alimentaires.
Origines et Développement d'une Collection Unique
Créée en 1945 à l'initiative de Roger n° 659, alors directeur de l'unité de recherche Cryptogamie du Muséum, la collection a été conçue dès le départ pour la conservation des espèces cultivables récoltées lors des missions des chercheurs de l'unité. Au fil du temps, elle s'est enrichie grâce à de nouvelles récoltes, des dons, des échanges et des acquisitions. Ces spécimens proviennent de récoltes sur le terrain, d'échanges avec d'autres institutions scientifiques et peuvent également être transmis par des correspondants extérieurs pour identification.
L'enrichissement de la collection suit la réglementation en vigueur, notamment le Protocole de Nagoya, et s'accroît d'environ 100 souches par an. Les objectifs sont doubles : élargir l'éventail des espèces disponibles et se focaliser sur des niches écologiques particulières, telles que les endophytes, les champignons du milieu fromager, ou encore les champignons des grottes. Cette approche permet de couvrir un large spectre de la biodiversité fongique et de répondre aux besoins spécifiques de la recherche contemporaine.
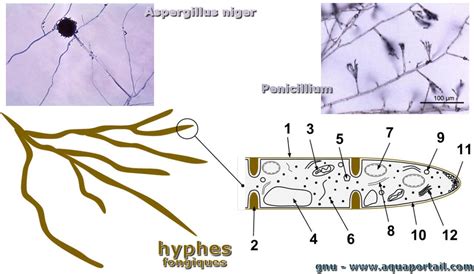
Méthodes de Conservation : De la Culture Vivante à la Cryoconservation
Initialement, les souches étaient maintenues en vie par repiquages successifs sur des milieux de culture artificiels. Cette méthode, bien qu'efficace pour la conservation à court terme, présentait des limites en termes de stabilité génétique et de risque de contamination. Aujourd'hui, les méthodes de conservation se sont considérablement améliorées. Toutes les souches sont désormais maintenues à l'état de vie latente par congélation. Cette technique permet de conserver les champignons récoltés il y a une soixantaine d'années dans un volume réduit, tout en garantissant qu'ils restent vivants et susceptibles d'être revivifiés, mis en culture, étudiés et utilisés pour des objectifs divers à tout moment.
La Collection LCP : Une Reconnaissance Européenne et Internationale
Au niveau européen, la collection est reconnue sous l'acronyme LCP et fait partie intégrante de l'European Culture Collection Organisation (ECCO). Sur la scène internationale, elle est enregistrée dans le World Data Center for Microorganisms (WDCM) sous le numéro 659, attestant de son importance et de sa conformité aux standards mondiaux.
MYCOBASE : La Base de Données au Service de la Recherche
Les données concernant toutes les souches sont informatisées et consultables sur la base de données MYCOBASE. Cette plateforme centralise des informations essentielles pour les chercheurs, facilitant l'accès et l'exploitation des ressources de la collection. Des données complémentaires, telles que les activités spécifiques, les séquences d'ADN, l'iconographie et la bibliographie, sont ajoutées au fur et à mesure de leur acquisition. Les deux premiers génomes complets de souches de la collection ont d'ailleurs été publiés en 2014, soulignant l'engagement de la collection dans les avancées génomiques.
Activités et Collaborations : Un Rôle Actif dans la Communauté Scientifique
La collection ne se contente pas de conserver ; elle est également un acteur dynamique de la recherche. Elle distribue en moyenne plus de 120 souches par an à des chercheurs issus de divers domaines tels que la systématique, la chimie et la génomique. Ces souches sont également mises à disposition d'enseignants et d'industriels pour la production de molécules utiles ou pour l'étude d'activités particulières, comme la dégradation enzymatique ou la résistance aux biocides.
Cette activité de distribution s'accompagne de collaborations étroites avec des organismes publics et privés, incluant des universités, l'INRA, et des industriels des secteurs agroalimentaire et cosmétique. La collection propose également un service d'identification des moisissures et de conseils, avec la possibilité de réaliser des prélèvements et des audits sur site. Cette expertise débouche régulièrement sur des contrats de recherche appliquée, portant par exemple sur l'épidémiologie des contaminations ou le criblage d'activités particulières. L'attrait pour le monde fascinant des moisissures s'étend même aux artistes, qui trouvent auprès de la collection un accompagnement pour leurs projets créatifs, qu'il s'agisse de films ou de sculptures vivantes.
Mutation des Souches Fongiques et Repiquages Successifs : Un Regard sur la Plasticité Génétique
Le maintien de cultures fongiques sur des milieux artificiels, bien que simplifié par les méthodes modernes de cryoconservation, soulève des questions fondamentales sur la stabilité génétique des souches au fil du temps et des générations. Les repiquages successifs, historiquement une pratique courante, pouvaient induire des mutations et des adaptations au milieu de culture. Comprendre ces processus est crucial, notamment dans le contexte de la recherche sur les mutations des souches fongiques.
La méthodologie génétique offre des outils puissants pour étudier le fonctionnement des systèmes biologiques. En perturbant un système, par exemple en altérant un gène, il devient possible d'observer les changements et d'en déduire la fonction de la pièce manquante. Dans le domaine de la mycologie, l'obtention de mutants présentant des défauts spécifiques est une étape clé pour élucider des processus biologiques.
Il existe deux approches principales pour obtenir ces mutants : la génétique classique (ou directe) et la génétique inverse (ou dirigée). La génétique classique démarre par la recherche de mutants sur la base de critères phénotypiques intéressants pour le processus étudié. Par exemple, des mutants d'auxotrophie pour la biosynthèse d'acides aminés, des mutants de longévité pour le vieillissement, ou des mutants bloqués à une étape embryonnaire pour l'analyse du développement. Cette étape de mutagenèse aboutit à l'obtention de mutants indépendants. Il faut ensuite caractériser ces mutations par les méthodes de la génétique classique. Par la suite, les gènes identifiés par ces mutations sont clonés par des approches de génétique moléculaire, telles que le clonage positionnel, par expression fonctionnelle, ou le séquençage complet des génomes des mutants. La formulation de modèles de fonctionnement repose sur la caractérisation fine des mutants, faisant appel à la biochimie, la biologie moléculaire, la cytologie, la génétique des interactions, et éventuellement la génétique inverse pour vérifier des hypothèses.
La génétique inverse, quant à elle, consiste à introduire des mutations spécifiques dans des gènes dont on connaît la séquence mais généralement pas le rôle. Ceci est réalisé in vitro à l'aide des techniques de l'ADN recombinant, puis ces gènes mutés sont réintroduits dans l'organisme par transformation ou transfection. Les effets observés sont ensuite analysés de la même manière que ceux obtenus par mutagenèse classique. La mutagenèse dirigée implique la création artificielle in vitro de mutations dans une séquence d'ADN connue, ou la construction de "cassettes" pour inactiver ou muter des gènes, suivie de leur introduction dans les cellules. Ces cassettes, une fois introduites, peuvent s'intégrer au sein des chromosomes de la cellule par recombinaison.
La Transformation des Champignons : Outils et Mécanismes
La transformation, c'est-à-dire l'introduction d'ADN exogène dans une cellule, est un processus fondamental pour la manipulation génétique des champignons. Chez les bactéries, la transformation naturelle est bien documentée, notamment chez Streptococcus pneumoniae et Escherichia coli, grâce à des systèmes protéiques spécifiques comme le système Com. Ces systèmes permettent l'entrée d'ADN sous forme de brin simple. Pour les bactéries moins compétentes, d'autres méthodes comme la conjugaison sont utilisées.
Chez les eucaryotes, y compris les champignons, la transformation naturelle est moins fréquente. Saccharomyces cerevisiae (levure) est une exception où une forme de transformation naturelle a été observée, expliquant potentiellement les transferts horizontaux de gènes observés dans les génomes eucaryotes. Cependant, pour la plupart des champignons filamenteux, il est nécessaire de rendre les cellules compétentes pour introduire de l'ADN.
Plusieurs méthodes sont employées :
- Transformation de protoplastes : Chez les organismes possédant une paroi cellulaire rigide, comme les levures ou les champignons filamenteux, l'élimination de la paroi par des enzymes permet d'obtenir des protoplastes. Ces cellules, dépourvues de paroi, sont plus facilement perméables à l'ADN.
- Traitement au PEG et/ou choc thermique : L'ajout de polyéthylène glycol (PEG) et/ou l'application d'un choc thermique peuvent déstabiliser les membranes cellulaires, facilitant l'entrée de l'ADN. L'ajout de cations comme Li+ ou Ca2+ peut agir en synergie.
- Électroporation : Cette technique utilise un choc électrique pour déstabiliser les membranes et permettre à l'ADN de pénétrer dans la cellule. Un protocole spécifique doit souvent être développé pour chaque espèce.
Pour les champignons filamenteux réfractaires à ces méthodes, la transformation médiée par Agrobacterium tumefaciens est une alternative. Cette bactérie, connue pour sa capacité à transférer naturellement de l'ADN aux plantes, peut être modifiée pour introduire des cassettes d'ADN dans les cellules fongiques. Le processus implique la construction d'un plasmide spécifique contenant des éléments nécessaires à la réplication dans E. coli et A. tumefaciens, ainsi qu'une région transférée délimitée par des frontières spécifiques, un marqueur de sélection et des sites de clonage.
Une autre méthode plus "brutale" est la transformation par biolistique, où des particules d'ADN sont projetées à haute vitesse sur les cellules.
🍄 La GÉNÉTIQUE et l'ÉPIGÉNÉTIQUE : Les SECRETS de la CULTURE des CHAMPIGNONS.
Sélections des Transformants et Destinés de l'ADN
L'efficacité de la transformation est souvent faible, ce qui rend nécessaire une étape de sélection des cellules ayant effectivement intégré l'ADN étranger. Deux stratégies de sélection principales sont couramment utilisées :
- Marqueur de résistance : L'ADN introduit porte un gène conférant une résistance à une substance toxique. Les cellules réceptrices sont sensibles à cette substance, permettant ainsi de ne sélectionner que les cellules transformées.
- Marqueur de biosynthèse : L'ADN contient un gène impliqué dans la biosynthèse d'un métabolite essentiel. Les cellules réceptrices sont mutées et déficientes pour ce métabolite (auxotrophes). Seules les cellules transformées, capables de produire le métabolite, peuvent survivre et se multiplier.
Une fois à l'intérieur de la cellule, l'ADN peut suivre différentes voies. S'il est sous forme de plasmide circulaire, il peut être répliqué s'il porte une origine de réplication (séquence ARS chez Saccharomyces cerevisiae). Les plasmides portant une séquence CEN sont mieux ségrégés lors des divisions cellulaires, assurant une répartition équitable. Chez de nombreux eucaryotes, les séquences ARS ne sont pas fonctionnelles, et il n'existe pas de plasmides nucléaires stables. Dans ce cas, l'ADN doit s'intégrer au génome pour être conservé. C'est ce qu'on appelle la transformation intégrative, qui se produit par des phénomènes de recombinaison.
La Recombinaison : Réorganisation du Génome Fongique
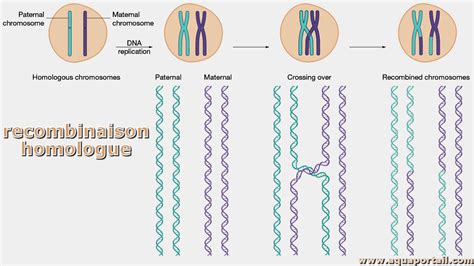
La recombinaison, au sens large, est la réorganisation du génome. Elle peut se produire par le brassage chromosomique lors de la méiose, ou plus spécifiquement par la cassure et le recollage des brins d'ADN, comme lors des crossing-over méiotiques. Les biologistes moléculaires distinguent trois grands types de recombinaison :
- Recombinaison homologue : Elle se produit entre des molécules d'ADN ayant des séquences identiques ou très proches. Elle nécessite généralement des régions d'homologie d'une cinquantaine à quelques centaines de paires de bases. Ce mécanisme est essentiel pour la réparation des cassures double brin de l'ADN et joue un rôle crucial dans la méiose pour générer de la diversité génétique.
- Recombinaison non-homologue : Ce type de recombinaison se produit entre des séquences d'ADN qui ne présentent pas d'homologie significative. Elle est souvent associée à des événements d'insertion ou de délétion de séquences d'ADN.
- Recombinaison spécifique à un site : Elle intervient entre des séquences d'ADN courtes et spécifiques, reconnues par des enzymes particulières.
La recombinaison homologue est particulièrement importante dans la réparation des cassures double brin. Lorsqu'une telle cassure survient, la cellule peut utiliser une molécule d'ADN homologue comme matrice pour réparer la cassure. Ce processus, via la formation et la résolution de jonctions de Holliday, peut conduire soit à une conversion génique, soit à un crossing-over, entraînant un échange de matériel génétique entre les molécules d'ADN. Chez Saccharomyces cerevisiae, la recombinaison homologue est le mécanisme principal de réparation des cassures double brin et est co-optée durant la méiose pour induire les crossing-over.
La Mutation Dirigée et l'Ingénierie Génétique chez les Champignons
L'avènement de la génomique et des techniques d'ADN recombinant a ouvert la voie à la mutagenèse dirigée chez les champignons. Cette approche permet de cibler précisément des gènes d'intérêt pour étudier leur fonction, ou pour améliorer des souches dans un but biotechnologique. Par exemple, des travaux ont porté sur l'amélioration de souches de Tolypocladium geodes pour la production de protéines recombinantes. Ces recherches ont impliqué des programmes d'amélioration génétique par sélection récurrente de mutants hyperproducteurs d'enzymes, suivis de mutagenèses par agents chimiques comme la N-méthyl-N'-nitro-N-nitrosoguanidine (NTG) ou l'éthylméthane sulfonate (EMS).
L'objectif était d'obtenir des souches avec des caractéristiques améliorées, comme une déficience en activités protéolytiques, ce qui est crucial pour éviter la dégradation des protéines recombinantes produites. Des mutants hyper-excréteurs de protéines ont été identifiés, capables de produire des concentrations significatives de protéines dans des milieux de culture simples. Ces avancées permettent d'envisager l'utilisation de champignons filamenteux comme des "usines cellulaires" pour la production de protéines hétérologues d'intérêt thérapeutique ou industriel.
Le développement de vecteurs d'expression fongiques et de marqueurs de sélection adaptés a été essentiel pour ces progrès. Des plasmides, tels que pUT703, pUT720, pUT771 et pUT760, ont été conçus et utilisés pour transformer des souches de Tolypocladium geodes. Ces plasmides portent des éléments régulateurs d'expression, comme le promoteur gpd d' Aspergillus nidulans, et des séquences signal synthétiques pour l'excrétion des protéines. La co-transformation, impliquant plusieurs plasmides, a permis d'introduire simultanément des gènes d'intérêt et des marqueurs de sélection.
L'étude de la biologie fondamentale des champignons, comme celle de Podospora anserina, a également bénéficié de ces approches. La transformation par cosmides porteurs d'informations génétiques a permis de révéler des mécanismes d'inactivation génique, tels que le phénomène rip (repeat-induced point mutation), ainsi que l'identification de nouveaux gènes impliqués dans la reproduction et le développement.
L'ensemble de ces recherches souligne l'importance de la collection de souches fongiques du MNHN comme point de départ pour des investigations approfondies sur la génétique, la biologie et les applications potentielles des champignons, allant de la compréhension des mécanismes moléculaires fondamentaux à la production biotechnologique de molécules d'intérêt.