Le cerveau de mammifère adulte est un organe d'une plasticité remarquable, capable de se modifier constamment en réponse aux stimulations environnementales changeantes. Ces modifications, induites par l'expérience, façonnent notre perception du monde qui nous entoure. Dans de nombreuses régions cérébrales, cette plasticité se manifeste par des altérations morphologiques des neurones, ainsi que par des changements dans le nombre et la position de leurs connexions. Ces ajustements anatomiques et fonctionnels sont les fondements de nos capacités d'apprentissage et de formation de la mémoire. Cependant, il existe deux régions cérébrales où cette plasticité atteint un niveau "extra-ordinaire" : l'hippocampe et le bulbe olfactif. Dans ces zones, la plasticité ne se limite pas à la modification des réseaux existants, mais inclut l'ajout de nouveaux neurones au sein de ces structures complexes. Ce phénomène est connu sous le nom de neurogenèse adulte.
Parmi ces deux sites de neurogenèse, le bulbe olfactif se distingue par l'afflux le plus conséquent de nouveaux neurones. Ces neurones bulbaires de novo proviennent de cellules souches qui, après division, donnent naissance à des neuroblastes, des neurones immatures. Ces derniers migrent ensuite vers le bulbe olfactif pour y subir leur maturation et devenir des neurones adultes fonctionnels. Bien que spatialement circonscrite dans le cerveau des mammifères, la neurogenèse adulte constitue un processus de plasticité accrue, essentiel à l'apprentissage et à l'encodage des informations.
Le Système Olfactif : Un Sens Souvent Sous-Estimé mais Crucial
Bien que l'olfaction soit parfois considérée comme le sens le moins important parmi nos cinq sens, son omniprésence dans notre vie quotidienne et son influence sur notre qualité de vie sont indéniables. Les odeurs ont le pouvoir de moduler nos humeurs, notre cognition et notre comportement. Ce sens est fondamental non seulement pour notre comportement alimentaire, car l'olfaction est un composant majeur de la perception de la flaveur des aliments en association avec la gustation et les entrées somatosensorielles, mais il joue également un rôle vital dans l'identification et l'évitement des dangers, tels que les incendies, les fuites de gaz ou la présence de prédateurs. De plus, l'olfaction est un acteur clé dans les interactions sociales et la reproduction.
Pour décrypter la myriade d'odeurs que nous percevons chaque jour, nous disposons d'un système olfactif remarquablement sophistiqué, capable de détecter, d'identifier et de discriminer une vaste gamme de stimuli olfactifs. Le traitement sensoriel des odeurs est un processus dynamique qui se déroule tout au long de notre vie, nécessitant des apprentissages constants et impliquant des mécanismes de plasticité cérébrale.
L'odorat et le goût - Réviser et comprendre la biologie, avec Cap'taine Snap
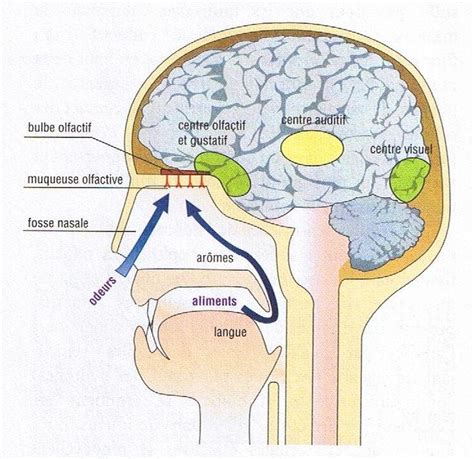
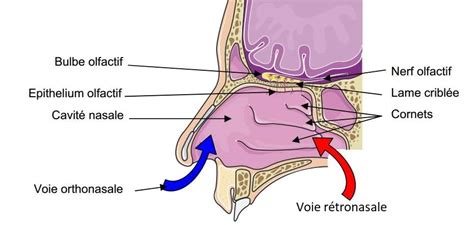
La perception olfactive s'articule schématiquement en trois étapes principales. Premièrement, une molécule odorante, une substance chimique volatile, atteint la cavité nasale par le biais de la respiration. Cette molécule se lie ensuite à des récepteurs olfactifs spécifiques situés sur les neurones sensoriels de l'épithélium olfactif, au fond de la cavité nasale. La reconnaissance entre l'odorant et le récepteur déclenche la conversion du message chimique de l'odeur en un message électrique. Deuxièmement, via les axones des neurones sensoriels, le message olfactif est transmis au bulbe olfactif, qui constitue le premier relais cérébral de l'information olfactive et le premier cortex sensoriel dédié à ce sens.
Le Bulbe Olfactif : Un Relais Clé et un Lieu de Plasticité Neuronale
Le rôle du bulbe olfactif est d'élaborer une représentation neurale de l'odorant à partir des signaux reçus des neurones sensoriels olfactifs de la cavité nasale. Il module également cette représentation en fonction des influences provenant d'autres régions cérébrales, puisque son activité est régulée par des voies neuromodulatrices cholinergiques, noradrénergiques et sérotoninergiques. Ces voies sont particulièrement importantes pour les processus d'attention et de mémoire.
Plus spécifiquement, le bulbe olfactif est composé de neurones relais, appelés cellules mitrales, qui reçoivent l'information olfactive via leurs connexions avec les neurones sensoriels. Ces cellules mitrales transmettent ensuite cette information aux structures cérébrales supérieures. L'information portée par les cellules mitrales est ensuite finement sculptée par de petits interneurones inhibiteurs avec lesquels elles sont connectées. Ces petits interneurones, tels que les interneurones périglomérulaires et les interneurones granulaires, sont précisément les cellules qui constituent la cible principale de la neurogenèse adulte dans le bulbe olfactif.
L'organisation du bulbe olfactif est caractérisée par la projection des axones des neurones sensoriels de l'épithélium olfactif vers le bulbe, où ils établissent des synapses avec les cellules mitrales. Au sein du bulbe olfactif, les cellules mitrales transmettent l'information aux centres supérieurs du cerveau. Deux populations d'interneurones modulent cette information : les interneurones périglomérulaires et les interneurones granulaires. De plus, des fibres neuromodulatrices influencent l'activité des interneurones inhibiteurs, jouant ainsi un rôle dans la régulation fine du traitement olfactif.
L'Histoire de la Neurogenèse Adulte : Du Dogme à la Réalité Scientifique
Le concept de neurogenèse adulte a une histoire fascinante, marquée par un dogme scientifique qui a prévalu pendant près d'un siècle. En 1906, le neurobiologiste espagnol Santiago Ramón y Cajal, lauréat du prix Nobel, a formulé un postulat selon lequel le cerveau adulte serait incapable de se régénérer. Il affirmait que "Une fois le développement terminé, la pousse et la régénération axonales et dendritiques s’arrêtent de manière irrévocable. Dans le système nerveux central adulte, le réseau nerveux est fixe, terminé et immuable". Selon cette vision, à la naissance, nous disposons d'un stock de neurones établissant entre eux de nouvelles connexions, mais il n'y aurait aucune apparition de nouveaux neurones chez l'adulte.
Ce postulat s'est imposé comme un dogme pendant près d'un siècle. Cependant, à partir des années 1960, de nombreuses certitudes concernant l'absence de neurogenèse chez l'adulte ont commencé à s'effondrer. Le chercheur américain Joseph Altman a découvert dans le cerveau de mammifères des cellules formées à l'âge adulte qui ressemblaient à des neurones. Ces cellules ont été formellement identifiées comme telles grâce à la microscopie électronique par Michael Kaplan quelques années plus tard (Altman, 1969). Longtemps ignorée, cette découverte a été confirmée dans les années 1990. Il est désormais établi que la neurogenèse persiste tout au long de la vie, principalement dans deux régions du cerveau de mammifère adulte : le gyrus denté de l'hippocampe et le bulbe olfactif. Cette neurogenèse a été décrite chez de nombreux mammifères, y compris chez l'homme, bien que la question de la neurogenèse olfactive chez l'humain fasse encore l'objet de discussions parmi certains auteurs.
Les Origines et la Migration des Nouveaux Neurones Olfactifs
La cellule souche, cellule totipotente capable de donner naissance à tous les types cellulaires, a été mise en évidence après la mise en culture de tissu neural de mammifère adulte. Les chercheurs ont observé que différentes régions du cerveau, notamment la zone sous-ventriculaire bordant les ventricules latéraux, étaient capables de former des "neurosphères", des amas de cellules pouvant se différencier en neurones ou en cellules gliales (Reynolds et Weiss, 1992). C'est précisément de cette région que proviennent les nouveaux neurones formés chez l'adulte dans le système olfactif.
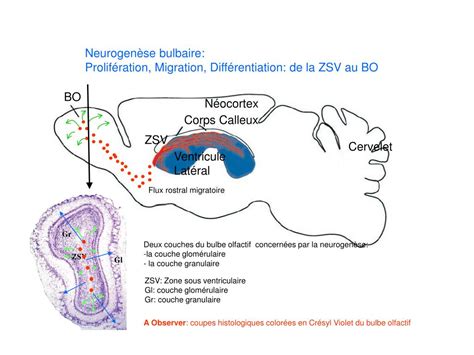
La cellule souche adulte présente dans la zone sous-ventriculaire se différencie en un neuroblaste (neurone immature). Ce neuroblaste migre ensuite pendant environ six jours le long d'un trajet très stéréotypé, appelé le flux rostral migratoire (RMS - Rostral Migratory Stream), pour atteindre le centre du bulbe olfactif. Une fois arrivé au bulbe, ces neuroblastes entreprennent une migration radiale pour rejoindre leur destination finale. Ils se différencient principalement en interneurones inhibiteurs granulaires (environ 94%) dans la couche granulaire, et en interneurones périglomérulaires (environ 4%) dans la couche glomérulaire (Lledo, Valley, 2016). Ainsi, des dizaines de milliers de nouveaux neurones arrivent et s'intègrent chaque jour au niveau du bulbe olfactif. Dans des conditions physiologiques normales, environ un mois après leur naissance, la moitié de ces neurones subit un phénomène d'apoptose (mort cellulaire programmée), tandis que l'autre moitié survit à plus long terme au sein du réseau neuronal bulbaire.
Maurice Curtis et ses collaborateurs ont apporté des éclaircissements importants sur la présence et l'organisation de ce flux migratoire chez l'homme. Ils ont observé que la neurogenèse et la migration des neuroblastes sont réduites dans la voie principale par laquelle les cellules de la zone sous-ventriculaire atteignent le bulbe olfactif chez les rongeurs. Dans ce contexte, le groupe de Maurice Curtis a découvert que chez l'humain, il existe une extension ventriculaire latérale qui s'étend jusqu'au bulbe olfactif, formant ainsi un "RMS humain". C'est par cette voie inattendue que les nouvelles cellules atteignent le bulbe olfactif.
Le Rôle Fonctionnel de la Neurogenèse Adulte dans l'Apprentissage Olfactif
Une question fondamentale qui découle de la découverte de la neurogenèse adulte concerne le rôle fonctionnel de ces nouveaux neurones dans le système olfactif. Compte tenu de l'implication du bulbe olfactif dans de nombreux apprentissages olfactifs et de sa forte activité neurogénique, l'hypothèse d'un rôle central de la neurogenèse dans les processus d'apprentissage a été avancée.
Plusieurs études ont démontré que l'activité olfactive, même simple (comme l'exposition à des odeurs), peut moduler le taux de formation de nouveaux neurones en influençant leur capacité à survivre dans le réseau préexistant (Mandairon et al., 2006b, Rochefort et al., 2002). Pour mieux cerner la signification fonctionnelle de la neurogenèse adulte, divers laboratoires ont étudié son rôle dans des contextes d'apprentissage et de mémoire. Le paradigme d'apprentissage le plus couramment utilisé est celui de l'apprentissage associatif de discrimination (un apprentissage explicite), où un animal apprend à associer une odeur spécifique à une récompense. Au fil des essais, l'animal améliore sa capacité à discriminer l'odeur pour obtenir sa récompense. Il a été observé que cet apprentissage est associé à une augmentation de la neurogenèse (Mandairon et al., 2006a, Sultan et al., 2010).
Grâce aux avancées en matière de vecteurs viraux, il est désormais possible de stimuler spécifiquement ces nouveaux neurones, ce qui entraîne une amélioration de la discrimination olfactive (Alonso et al., 2012). Les nouveaux neurones qui sont sélectionnés pendant le processus d'apprentissage deviennent alors le support de la trace mnésique. Par conséquent, leur suppression pharmacologique, génétique ou par irradiation entraîne un déficit de la mémoire (Imayoshi et al., 2008, Lazarini et al., 2009, Sultan et al., 2010). Inversement, l'effacement d'une mémoire associée à une odeur provoque la suppression prématurée de ces neurones (Sultan et al., 2011).
En plus de l'apprentissage associatif, il existe également l'apprentissage perceptif, qui concerne l'amélioration de la capacité à distinguer des stimuli subtilement différents. La neurogenèse adulte joue un rôle crucial dans ce type d'apprentissage en permettant au système olfactif de s'adapter à de nouvelles expériences et d'affiner sa perception.
Facteurs Modulant la Neurogenèse et Plasticité du Bulbe Olfactif
L'olfaction, bien que souvent négligée, est un sens dynamique et interactif. Les odeurs influencent notre humeur, nos émotions et nos comportements sociaux. Le système olfactif est constamment sollicité pour analyser et interpréter un flot continu d'informations olfactives. Ce traitement sensoriel dynamique, rendu possible par la neurogenèse adulte, est cependant susceptible d'être perturbé.
Le stress et la pollution sont deux facteurs environnementaux reconnus pour altérer la neurogenèse adulte et, par conséquent, perturber notre perception des odeurs. Le stress chronique, par exemple, peut entraîner une diminution de la prolifération des cellules souches et de la survie des nouveaux neurones dans le bulbe olfactif, affectant ainsi la plasticité du système et la capacité à apprendre de nouvelles odeurs ou à se souvenir d'expériences olfactives passées. De même, l'exposition à certains polluants peut avoir des effets toxiques sur les cellules neurogéniques, compromettant ainsi le renouvellement neuronal.
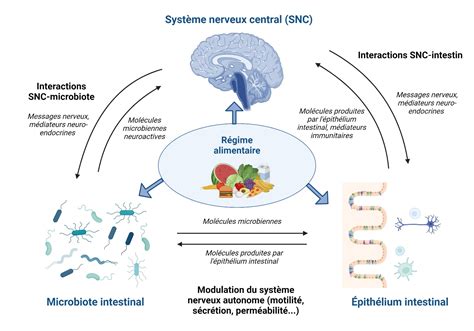
Ces altérations peuvent avoir des conséquences significatives sur notre qualité de vie, affectant notre capacité à apprécier la nourriture, à détecter des dangers potentiels ou à interagir socialement. La compréhension des mécanismes par lesquels le stress et la pollution affectent la neurogenèse est donc essentielle pour développer des stratégies visant à préserver la fonction olfactive.
Le Bulbe Olfactif Accessoire et son Rôle Spécifique
Il est important de distinguer le bulbe olfactif principal du bulbe olfactif accessoire. Le bulbe olfactif accessoire est une structure distincte, située dans la région dorsale-postérieure du bulbe olfactif, particulièrement développée chez les macrosmates (animaux ayant un odorat très développé, comme le rat). Il forme un système sensoriel parallèle et indépendant du traitement des odeurs par le bulbe olfactif principal. Sa fonction principale est de recevoir des informations de l'organe voméronasal, un épithélium spécialisé de la cavité nasale, qui est particulièrement sensible à la détection des phéromones et d'autres stimuli chimiques.
Comme le bulbe olfactif principal, le bulbe olfactif accessoire contient des glomérules où les récepteurs olfactifs forment des synapses avec les cellules mitrales. Cependant, les cellules mitrales du bulbe olfactif accessoire projettent leurs axones vers l'amygdale et l'hypothalamus, et non vers le cortex olfactif. Ce système olfactif accessoire est impliqué dans les comportements liés à l'agression et à la reproduction. Bien que cette structure ne soit pas présente de manière distincte chez l'adulte humain, le bulbe olfactif principal peut assumer certaines de ses fonctions. Des expériences suggèrent que des capacités de reconnaissance olfactive mère-enfant chez l'humain, ou encore des influences sur le choix d'un partenaire chez la femme, pourraient être assimilées à la présence d'un système olfactif accessoire.
Anomalies et Pathologies Affectant le Bulbe Olfactif
Bien que le bulbe olfactif soit une structure remarquablement résiliente, il n'est pas à l'abri de certaines anomalies et pathologies. La dégénérescence bulbaire est décrite dans diverses maladies neuro-évolutives telles que la maladie d'Alzheimer et la maladie de Parkinson. De plus, certains troubles neuropsychiatriques sont également associés à une régression bulbaire observable lors d'analyses spécifiques.
Des cas rares mais fascinants d'individus dépourvus de bulbe olfactif ont été rapportés. Une équipe israélienne de l'Institut Weizmann des Sciences a identifié deux femmes, toutes deux gauchères et possédant une jumelle, qui présentaient un sens de l'odorat normal malgré l'absence de bulbe olfactif. Ces cas exceptionnels soulèvent des questions sur la redondance fonctionnelle au sein du système olfactif et sur la capacité du cerveau à compenser l'absence de structures majeures.
Il est également intéressant de noter que certaines structures présentes pendant l'embryogenèse, qui jouent un rôle dans la reconnaissance olfactive précoce, peuvent disparaître ou s'intégrer au bulbe olfactif principal chez l'adulte. Par exemple, le complexe glomérulaire modifié, composé d'une dizaine de très gros glomérules, permettrait au nouveau-né de reconnaître sa mère parmi les autres individus du groupe. On pense également que l'organe voméronasal, composé de quelques cellules olfactives situées dans la cloison nasale, est présent peu avant la naissance du bébé humain. En raison de leur position profonde, il y a peu d'images montrant des anomalies bulbaires directement liées à des neuropathies.
En résumé, la neurogenèse du bulbe olfactif humain représente un domaine de recherche dynamique et essentiel pour comprendre la plasticité cérébrale, l'apprentissage et la mémoire olfactive. Ce phénomène, loin d'être une relique du développement, est un processus actif qui contribue à notre capacité d'interagir avec le monde des odeurs tout au long de notre vie.
tags: #neurogenesis #olfactif #bulb #human