Le sulfamate d'ammonium, une substance chimique aux propriétés remarquables, a suscité un intérêt considérable au fil des ans pour ses diverses applications, allant du désherbage sélectif à son utilisation comme ignifugeant. Bien qu'il ait été un outil précieux pour lutter contre des plantes difficiles et envahissantes, son statut réglementaire a évolué, notamment en Europe, où son utilisation comme biocide est désormais interdite, du moins provisoirement. Cet article explore en détail le sulfamate d'ammonium, ses applications historiques et actuelles, ses mécanismes d'action, sa toxicité potentielle et les considérations réglementaires qui encadrent son usage.

Un Désherbant Puissant aux Multiples Cibles
Le sulfamate d'ammonium est avant tout reconnu pour sa puissante action phytocide, c'est-à-dire sa capacité à détruire les plantes. Son efficacité réside dans son action systémique, affectant toutes les parties de la plante, que ce soit par contact direct avec le feuillage, les racines, ou même par pénétration dans le bois via des incisions pratiquées sur les troncs. Cette polyvalence d'application en faisait un allié de choix pour s'attaquer à des espèces végétales réputées coriaces, notamment celles qui présentent une résistance accrue à d'autres désherbants plus couramment utilisés, comme le glyphosate.
Historiquement, le sulfamate d'ammonium a été employé pour venir à bout de problématiques végétales telles que la Renouée du Japon, une plante invasive particulièrement tenace, ainsi que pour le contrôle des ligneux, des ronciers envahissants, et des souches d'arbres et de ronces, empêchant ainsi leur repousse. Son utilisation s'étendait également à des applications plus spécifiques, comme le traitement par injection dans la sève d'arbres indésirables, une méthode qui a été interdite en Europe depuis le 28 mars 2007, le traitement basal étant quant à lui interdit depuis le 3 février 2006. Le badigeonnage pour le désouchage chimique en sylviculture était également une pratique courante, mais elle est aujourd'hui interdite en Europe. Ces méthodes étaient particulièrement utiles pour la réouverture de milieux naturels envahis par la végétation, comme cela a été testé avec succès sur certains chantiers menés par des organisations telles que le British Trust for Conservation Volunteers, English Heritage, le National Trust, ainsi qu'en bordure de voies ferrées ou de voies navigables.

Mécanismes d'Action Phytocide
L'efficacité du sulfamate d'ammonium repose sur sa capacité à perturber les processus physiologiques essentiels de la plante. Appliqué par pulvérisation foliaire, il est absorbé par les feuilles et transporté à travers la plante, atteignant les racines et inhibant leur croissance. Il peut également être appliqué directement sur les coupes de bois ou les souches, où il est absorbé par le xylème, empêchant ainsi la régénération de la plante.
Une méthode d'application spécifique pour la Renouée du Japon implique la pulvérisation sur la base des tiges préalablement coupées à environ 30 cm du sol. Une solution concentrée, à raison de 400 grammes par litre, est injectée à la base des tiges. Une autre approche consiste à placer un amas de cristaux de sulfamate d'ammonium juste au-dessus de la base des tiges fraîchement coupées, bien que cette méthode présente un risque accru d'intoxication pour les animaux.
Une fois appliqué, le sulfamate d'ammonium est progressivement dégradé dans le sol, en l'espace de 3 à 4 mois en climat tempéré, pour se transformer en sulfate d'ammonium. Ce dernier est une forme d'azote assimilable par les plantes, généralement considérée comme sans danger pour l'environnement une fois transformée.
Une mise en évidence expérimentale de transfert d'azote
Un Produit Chimique aux Applications Industrielles Diverses
Au-delà de son rôle de désherbant, le sulfamate d'ammonium trouve également sa place dans plusieurs secteurs industriels. Sa capacité à agir comme retardateur de flamme est l'une de ses propriétés les plus exploitées. À l'instar d'autres sels d'ammonium comme le dihydrogénophosphate d'ammonium ou le sulfate d'ammonium, il offre une alternative intéressante aux retardateurs de flamme à base de métaux ou de minéraux, notamment en raison de sa solubilité dans l'eau. Sa température de décomposition relativement basse le rend particulièrement adapté pour ignifuger les matériaux à base de cellulose, tels que le papier et le bois.
Dans l'industrie, le sulfamate d'ammonium est également utilisé comme plastifiant, dans les processus de galvanoplastie, et comme réactif de laboratoire. Il entre dans la composition de certains produits chimiques destinés à la fabrication de molécules organiques.
Une autre application notable est son rôle d'« accélérateur » de compostage, particulièrement dans les composts industriels qui traitent des quantités importantes de déchets végétaux, y compris des racines de plantes potentiellement capables de reprendre vie. En fournissant de l'azote, il stimule l'activité des micro-organismes responsables de la décomposition, accélérant ainsi le processus de transformation en humus.
Le Sulfamate d'Ammonium et le Sulfate d'Ammonium : Distinctions et Relations
Il est important de distinguer le sulfamate d'ammonium du sulfate d'ammonium, bien qu'ils soient chimiquement liés et que le premier se dégrade en le second dans le sol. Le sulfate d'ammonium est un engrais azoté à action rapide, contenant environ 21% d'azote sous forme d'ammonium (NH4+) et 24% de soufre sous forme de sulfate (SO42-). Il est largement utilisé pour favoriser la croissance des plantes et, de manière intéressante, pour contrôler la mousse dans les pelouses. Sa teneur élevée en azote contribue à un gazon luxuriant et d'un vert profond. Le sulfate d'ammonium possède également un effet acidifiant, ce qui le rend particulièrement utile pour les sols alcalins.

Les essais menés par ARVALIS - Institut du végétal entre 2010 et 2012 ont mis en évidence l'intérêt du sulfate d'ammonium, sous le nom commercial d'Actimum, lorsqu'il est ajouté à des associations d'herbicides antigraminées et d'huiles. Il a permis un gain d'efficacité moyen de 10 à 11 points, et dans certains cas, ce gain a pu dépasser 30 points. Ces gains d'efficacité semblent indépendants du niveau d'infestation en adventices. Les hypothèses avancées pour expliquer cet effet « dopant » incluent la limitation de la dessiccation des gouttes pulvérisées en cas d'hygrométrie faible, un effet « pénétrant » similaire à celui des huiles, ou encore un effet « étalant » comparable à celui des mouillants. Il est toutefois souligné que le sulfate d'ammonium ne remplace pas l'huile dans ces formulations.
Réglementation et Sécurité : Un Cadre en Évolution
En Europe, l'utilisation du sulfamate d'ammonium en tant que biocide est désormais interdite, du moins de manière provisoire. Cette interdiction a conduit au retrait de nombreuses autorisations de mise sur le marché. En France, les sociétés détentrices ont été notifiées de ces décisions, et des délais ont été accordés pour l'écoulement des stocks et l'utilisation par les particuliers et les professionnels. Les produits concernés qui restent en possession des distributeurs ou des utilisateurs après les dates limites deviennent, aux yeux de la loi, des déchets. Le détenteur de ces déchets est alors responsable de leur élimination dans le respect de la législation en vigueur.
Il est à noter qu'en tant qu'intrant chimique, le sulfamate d'ammonium n'a jamais été autorisé en agriculture biologique.
Malgré son interdiction en tant que biocide, il y a quelques années, la Henry Doubleday Research Association (HDRA), un groupe spécialisé dans le jardinage biologique (également connue sous le nom de Garden Organic), a publié un article relatant des succès dans la lutte contre des plantes invasives grâce au sulfamate d'ammonium, le proposant comme une alternative lorsque d'autres solutions s'avéraient insuffisantes.
Le sulfamate d'ammonium n'étant pas réputé pour sa toxicité environnementale immédiate, il n'a pas fait l'objet d'études de toxicité approfondies. Cependant, le manque d'études complètes au moment du renouvellement des autorisations a soulevé des questions sur d'éventuels effets environnementaux directs ou indirects, immédiats ou différés, sur la faune, la flore et la fonge sauvage, ainsi que sur les écosystèmes.
Précautions d'Usage et Toxicité
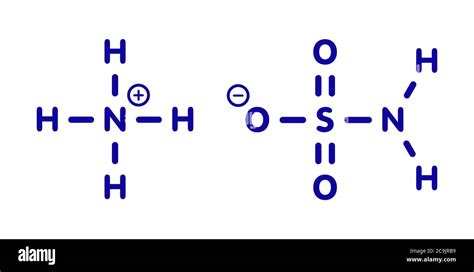
Le sulfamate d'ammonium est un solide cristallin blanc, facilement soluble dans l'eau. Sa formule chimique est H6N2O3S et sa masse moléculaire est de 114,1 g/mol. C'est une substance hygroscopique qui se dissout très bien dans l'eau (2800 g/L). Sa température de fusion est de 131°C, et sa décomposition débute vers 160°C, libérant des gaz tels que des composés d'ammonium, des oxydes d'azote et des oxydes de soufre.
Concernant sa toxicité pour l'homme, le sulfamate d'ammonium provoque des irritations au niveau de la peau, des yeux et des voies respiratoires. Les symptômes peuvent inclure des rougeurs, des douleurs oculaires et une gêne respiratoire. En cas d'inhalation, il est recommandé de protéger les voies respiratoires. La concentration dans l'air du milieu de travail ne doit pas dépasser la Valeur Limite d'Exposition Professionnelle (VEMP) de 10 mg·m-3 d'air. Si cette concentration est dépassée, le port d'un appareil de protection respiratoire adapté est nécessaire. Pour des concentrations allant jusqu'à 50 mg·m-3, un appareil de protection respiratoire à particules peut suffire. Au-delà, des masques plus performants, voire des appareils autonomes, sont recommandés.
Aux doses habituelles d'utilisation comme désherbant, il n'est généralement pas considéré comme nécessaire d'éloigner les enfants et les animaux des zones traitées. Cependant, une méthode d'application consistant à placer des cristaux sur des tiges fraîchement coupées présente un risque d'intoxication pour les animaux.
Le stockage du sulfamate d'ammonium doit se faire dans des récipients hermétiques, dans un lieu frais, sec et ventilé, à l'abri des matières oxydantes, acides ou alcalines. Il n'est pas inflammable, mais en cas d'incendie impliquant ce produit, le port d'un appareil respiratoire autonome et de vêtements protecteurs est recommandé.
Premiers Secours et Gestion des Risques
En cas de contact accidentel, les mesures de premiers secours sont les suivantes :
- Inhalation : Transporter la victime à l'air frais, la mettre au repos et surveiller médicalement si les symptômes persistent.
- Contact oculaire : Rincer abondamment à l'eau claire pendant au moins 5 minutes. Retirer les lentilles de contact si possible.
- Contact cutané : Laver immédiatement à l'eau et au savon.
- Ingestion : Rincer la bouche et consulter un médecin si des symptômes apparaissent.
Les données de toxicité aiguë indiquent une DL50 (dose létale médiane) de 2000 mg·kg-1 chez le rat par voie orale, et de 3100 mg·kg-1 chez la souris par voie orale.
Incompatibilités Chimiques
Le sulfamate d'ammonium peut réagir avec des agents oxydants puissants, créant des risques d'inflammation ou d'explosion. Il est également incompatible avec les acides forts, avec lesquels il peut générer des réactions exothermiques dangereuses. En présence d'alcalis ou en solution aqueuse, il peut se décomposer en libérant de l'ammoniac gazeux, ce qui peut créer une atmosphère toxique dans les espaces confinés. L'hydrolyse en solution aqueuse conduit à la formation de sulfate d'ammonium.
Conclusion Provisoire sur un Produit en Transition
Le sulfamate d'ammonium demeure une substance aux propriétés chimiques et biologiques intéressantes. Son efficacité comme désherbant puissant contre les plantes difficiles, son rôle dans diverses applications industrielles, notamment comme retardateur de flamme et accélérateur de compost, en font un produit aux multiples facettes. Cependant, son statut réglementaire en Europe, marqué par une interdiction progressive de son utilisation comme biocide, souligne une prise de conscience accrue des risques potentiels pour l'environnement et la santé humaine, même si les études approfondies sur ses effets à long terme font encore défaut. L'évolution des réglementations et la recherche d'alternatives plus sûres continueront de façonner l'avenir de ce composé chimique.